Здесь есть кто-нибудь, кто хорошо разбирается в химии? Мне нужна помощь: взаимодействует ли гидроксид цинка с серной кислотой (Zn(OH)2 + H2SO4 = ?) и, если да, то, что при этом получается. Укажите основные физические и химические свойства полученного соединения, а также способы его получения. Заранее, благодарю!
В результате взаимодействия гидроксида цинка с серной кислотой (Zn(OH)2 + H2SO4 = ?) происходит образование средней соли – сульфата цинка и воды. Молекулярное уравнение реакции имеет вид:
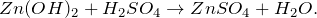
Запишем ионные уравнения, учитывая, что гидроксид цинка и вода на ионы не распадаются, т.е. не диссоциируют.
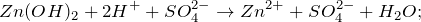
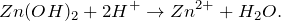
Первое уравнение называют полным ионным, а второе – сокращенным ионным.
Сульфат цинка представляет собой кристаллы белого цвета, разлагающиеся при сильном нагревании. Он хорошо растворяется в воде (гидролизуется по катиону). Реагирует с концентрированной серной кислотой, щелочами, гидратом аммиака. Вступает в реакции обмена и комплексообразования.
Фосфорные удобрения Более половины выпуска фосфорных удобрений в настоящее время производится в СЗФО. По итогам полугодия 2019 г. доля рынка СЗФО составила 54%.
Наиболее высокие показатели по объемам выпуска азотных удобрений по итогам полугодия 2019 г. зафиксированы в Приволжском ФО, доля рынка 34%. В число крупных ком.
Производство серной кислоты налажено на предприятиях цветной металлургии, которые выпускают серную кислоту из отходящих газов. Основными поставщиками H2SO4 на внутренний рынок России.
Производственные показатели аммиачной отрасли растут ежегодно, покрывая растущие потребности внутреннего спроса на производство азотных удобрений. Не стоит забывать, что аммиак также.
Жители Кавказских Минеральных Вод собирают подписи против строительства завода нитроцеллюлозы в городе Лермонтове Ставропольского края, пишет NewsTracker. Сбор подписей ведется как в интернете.
В Балашовском районе Саратовской области сегодня состоялась церемония закладки камня на месте строительства завода по глубокой переработке пшеницы "Саратовские Биотехнологии". В ней принял участие .
Производители фосфорных, калийных и сложных удобрений
Производители азотных удобрений
Производители серной кислоты в России
Производители фосфорных, калийных и сложных удобрений
Производители азотных удобрений
Производители серной кислоты в России
Основная продукция: цинк металлический чушковой марки Ц-3, кадмий, штейн медный, кислота серная, белила цинковые сухие, пыль высокотемпературного обжига цинковых концентратов (всего 2-5 тыс. тонн в год).
Торговая фирма, специализирующаяся на купле-продаже технической химии: 1. Кислота соляная 2. Кислота серная 3. Кислота ортофосфорная 4. Кислота азотная 5. Этиленгликоль 6. Натр едкий 7. Перекись водор.
Руководитель Чуб Владимир Евгеньевич Продукция: кокс, кокс доменный, кокс-орех, бензол, газ коксовый, кислота серная, концентрат германия.
Компания занимается добычей меди и вермикулита в районе р. Лимпопо и является единственным в Южной Африке производителем рафинированной меди. Основным продуктом компании является медь наряду с побочны.
Atlantic Copper — один из важнейших в мире производителей меди. Благодаря инвестициям и модернизации производственного процесса, в настоящее время компания способна производить около 310 тыс.т. медных.
Среднеуральский медеплавильный завод (СУМЗ), отметивший в 2000 году свое 60-летие, является крупнейшим на Урале предприятием по выплавке меди из первичного сырья, производству из отходящих металлургич.
Предлагаем кислоту азотную хч со склада в г. Саратов. Фасовка-канистры по 20 л ( 28 кг) .Цена 53 руб/кг.
Продам промышленную химию и химическое сырьё. Амины, гидроксиды, гликоли, кислоты, ПАВы, пластификаторы, растворители, соли, спирты, эфиры и др. Изопропиловый спирт, Гипохлорит натрия, Глицерин дистил.
С 1929 года производим: — фосфатные соли натрия, калия, кальция — пищевую фосфорную кислоту 73% и 85% Всего более 30 видов продукции (фосфатные добавки, ортофосфаты, цитраты, лимонная кислота и т.д.
Реализуем ортофосфорную кислоту для промышленного применения V не менее 73%, So3 не более 3%, As не более 0, 004 % Отгрузка ЖД цистернами. Цена на жд станции покупателя по запросу.
1. КРАТКАЯ ХАРАКТЕРИСТИКА 1.1. ПАЛЬМИТИНОВАЯ КИСЛОТА, ЕЁ СОЛИ И ЭФИРЫ 1.1.1. Пальмитиновая кислота (Цетиловая) 1.1.2. Соли пальмитиновой кислоты (пальмитаты) 1.1.3. Эфиры пальмитиновой кислоты (п.
Организация предлагает со склада в г. Саратов кислоту лимонную пищевую производства Китай. Фасовка-мешки по 25 кг. Скидки от объемов, возможна доставка по городу. Адреса складов в г. Саратов: пос. З.
Составляем уравнение реакции взаимодействия веществ в молекулярной форме:
По таблице растворимости солей в воде устанавливаем, что к сильным электролитам относятся растворимые в воде соли CuSO4 и Na2SO4, Cu(OH)2 – малорастворимое соединение, NaOH – сильный электролит (приложение, табл.2).
Составим полное ионно-молекулярное уравнение, записав растворимые соли и сильное основание в виде ионов, а осадок Cu(OH)2 в виде молекулы:
Cu 2+ + SO4 2– + 2Na + + 2OH – = Cu(OH)2 + 2Na 2+ + SO4 2–
Исключаем из обеих частей полного ионно-молекулярного уравнения одинаковые ионы



 Cu 2+ + SO4 2– + 2Na + + 2OH – = Cu(OH)2 + 2Na 2+ + SO4 2–
Cu 2+ + SO4 2– + 2Na + + 2OH – = Cu(OH)2 + 2Na 2+ + SO4 2–
Записываем сокращенное ионно-молекулярное уравнение:
Пример 2.Составьте молекулярное и ионно-молекулярное уравнения, которые доказывают амфотерный характер гидроксида цинка.
Для доказательства амфотерного характера гидроксида цинка необходимо привести уравнения реакций, в которых это соединение проявляет основные и кислотные свойства.
Основные свойства гидроксид цинка проявляет при взаимодействии с растворами кислот. Например с серной кислотой
При составлении полного ионно-молекулярного уравнения в виде ионов записываем сильную кислоту H2SO4, растворимую соль ZnSO4, слабый электролит Н2О и малорастворимое основание записываем в молекулярном виде:
Исключив из обеих частей уравнения одинаковые ионы, получаем сокращенное ионно-молекулярное уравнение
Кислотные свойства гидроксид цинка проявляет при взаимодействии с растворами щелочей (NaOH, KOH):
В полном ионно-молекулярном уравнении в виде ионов записываем сильное основание NaOН и растворимую комплексную соль:
Zn(OH)2 + 2Na + + 2OH – = 2Na + + [Zn(OH)4] 2–
Сокращенное ионно-молекулярное уравнение имеет вид
Составление молекулярных уравнений
по ионно-молекулярным
Чтобы составить молекулярное уравнение по сокращенному ионно-молекулярному, необходимо определить, какой сильный электролит соответствует каждому иону, так как ионы – это остатки сильных электролитов.
Пример. Составьте по два молекулярных уравнения, которые выражаются следующим ионно-молекулярным уравнением:
Решение. При составлении молекулярных уравнений следует подобрать к ионам Zn 2+ и СО3 2– сильные электролиты: